
Creare cellule sintetiche dai costituenti fondamentali. Realizzate con un approccio bottom up, le cellule sintetiche e altre strutture molecolari necessarie agli organismi viventi stanno iniziando a funzionare, e presto potrebbero fornire un test fondamentale sui confini della vita.
C’erano solo otto ingredienti: due proteine, tre agenti tampone, due tipi di molecole di lipidi e una certa dose di energia chimica. Ma questo è stato sufficiente per creare una flottiglia di ammassi pulsanti, strutture rudimentali simili a cellule dotate di alcuni dei meccanismi necessari per dividersi per conto proprio.
Per la biofisica Petra Schwille, queste creature danzanti nel suo laboratorio rappresentano un passo importante verso la costruzione di una cellula sintetica con approccio “dal basso verso l’alto” (bottom–up), qualcosa a cui ha lavorato negli ultimi dieci anni, e più di recente al Max-Planck-Institut per la biochimica a Martinsried, in Germania. “Sono sempre stata affascinata da questa domanda: ‘Che cosa distingue la vita dalla materia non vivente?’”, spiega la ricercatrice. La sfida, secondo Schwille, è determinare quali componenti sono necessari per realizzare un sistema vivente. Nella sua perfetta cellula sintetica, lei conoscerebbe ogni singolo fattore che la fa funzionare.
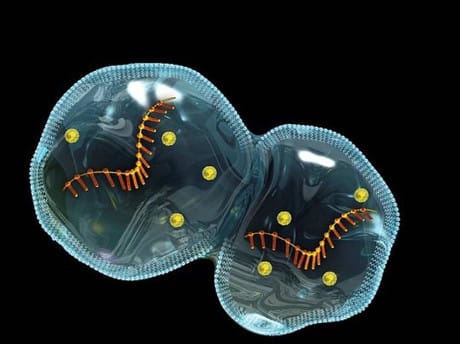
I ricercatori hanno cercato di creare cellule artificiali per più di vent’anni, mettendo insieme le biomolecole nel giusto contesto per approssimare i diversi aspetti della vita. Sebbene siano numerosi, generalmente questi aspetti rientrano in tre categorie: compartimentazione o separazione delle biomolecole nello spazio; metabolismo, cioè la biochimica che sostiene la vita; controllo dell’informazione, archiviazione e gestione delle istruzioni cellulari.
Il passo degli studi è accelerato, grazie in parte ai recenti progressi nelle tecnologie microfluidiche, che permettono agli scienziati di coordinare i movimenti di minuscole componenti cellulari. I gruppi di ricerca hanno già identificato modi con cui è possibile plasmare ammassi simili a cellule nelle forme desiderate, creare versioni rudimentali del metabolismo cellulare e trapiantare in cellule viventi i genomi prodotti artificialmente. Ma mettere insieme tutti questi elementi rimane una sfida.
Nonostante ciò, il settore è pervaso da un nuovo senso di ottimismo riguardo all’impresa. A settembre 2017, ricercatori di 17 laboratori nei Paesi Bassi hanno formato il gruppo Building a Synthetic Cell (BaSyC), che entro dieci anni punta a costruire “un sistema simile alla cellula, in grado di crescere e dividersi”, secondo il biofisico Marileen Dogterom, che dirige BaSyC e un laboratorio alla Delft University of Technology.
A settembre, la statunitense National Science Foundation (NSF) ha annunciato il suo primo programma sulle cellule sintetiche, finanziato per con importo di dieci milioni di dollari. E numerosi ricercatori europei, inclusa Schwille, hanno proposto di costruire una cellula sintetica nell’ambito della Future and Emerging Technologies Flagship della Commissione Europea, che riceve un miliardo di euro di finanziamenti.
Tutto nella confezione
I gruppi di ricerca hanno compiuto grandi passi avanti nel ricreare diversi aspetti della vita di una cellula, specialmente nell’imitare le membrane che circondano le cellule e nel dividere in compartimenti le componenti interne. Questo perché organizzare le molecole è la chiave per farle funzionare insieme nel momento e nel posto giusto. Anche se è possibile aprire un miliardo di batteri e versare il contenuto in una provetta, per esempio, i processi biologici non continueranno per molto tempo. Alcuni componenti devono essere tenuti separati e altri insieme.
“Per me, si tratta di sociologia delle molecole”, afferma Cees Dekker, biofisico del alla Delft University of Technology.
Nella maggior parte dei casi, questo significa organizzare biomolecole su membrane lipidiche o all’interno di esse. Schwille e il suo gruppo sono esperti di membrane. Da circa dieci anni, il gruppo ha iniziato ad aggiungere proteine Min, che dirigono il macchinario addetto alla divisione in una cellula batterica, a fogli di membrana lipidiche artificiali. Le Min, hanno scoperto i ricercatori, spuntavano dentro e fuori dalle membrane, facendole ondeggiare e roteare. Ma quando hanno aggiunto le proteine a sfere lipidiche 3D, le strutture sono scoppiate come bolle di sapone, dice Schwille. Il suo gruppo e altri hanno superato questo problema usando tecniche microfluidiche per costruire contenitori di membrana con dimensioni cellulari, o liposomi, che possono tollerare più inserimenti di proteine nelle membrane stesse o al loro interno.
Un borsista di Schwille, Thomas Litschel, e i suoi collaboratori hanno disciolto le proteine Min in acqua e rilasciato gocce della miscela in una provetta in rapida rotazione. La forza centrifuga tira le gocce attraverso strati di lipidi densi che le incapsulano lungo il percorso. Esse riappaiono dalla parte opposta in forma di liposomi che misurano 10-20 micrometri in tutto, circa le dimensioni di una cellula animale o vegetale media. Questi liposomi, noti come vescicole unilamellari giganti (GUV), possono essere ottenuti in modi diversi, ma nelle mani di Litschel, le proteine Min hanno indotto le GUV a pulsare, fluttuare in giro e contrarsi al centro.
Il gruppo di Schwille vuole capitalizzare la propria conoscenza di queste proteine, che possono produrre modelli di membrana e auto-organizzarsi. “Capiamo queste molecole molto bene”, dice. “Vorremmo vedere che cosa possiamo ottenere con elementi relativamente semplici come le Min”. Forse, come suggerisce il lavoro di Litschel, il gruppo potrebbe usare le proteine per dare forma a membrane per divisione o per aggregare le componenti all’estremità di una cellula sintetica. Proprio come alcuni fisici potrebbero usare nastro adesivo e carta stagnola per mettere a punto i loro esperimenti, Schwille spera che queste molecole biologiche già disponibili le daranno la possibilità di armeggiare con strutture simil-cellulari: “Sono uno sperimentatrice fino all’osso”.
I membri del gruppo di Dekker hanno anche riempito i liposomi con le loro proteine preferite usando un chip microfluidico (si veda questa infografica). Sul chip, due canali contenenti molecole lipidiche convergono su un canale pieno d’acqua ed emettono liposomi di dimensioni cellulari che possono contenere varie molecole biologiche, in grado di attraversare la membrana o rimanere liberamente fluttuanti all’interno del contenitore.
Il suo gruppo ha sperimentato pressurizzazione, deformazione e rimodellamento dei liposomi per ottenere forme non sferiche che imitano meglio le cellule. I dispositivi microfluidici offrono ai ricercatori un maggiore controllo per spostare, ordinare e manipolare i liposomi usando micro-canali che funzionano quasi come circuiti. Quest’anno, il laboratorio di Dekker ha progettato un chip in grado di dividere meccanicamente un liposoma in due spingendolo contro una sporgenza appuntita.

”Ovviamente, non è quello che cerchiamo: vogliamo dimostrare la divisione cellulare che procede dall’interno, ma ci fornisce comunque informazioni interessanti”, afferma Dekker. Queste informazioni includono la forza che serve per dividere una cellula e quali tipi di manipolazione fisica possono tollerare i liposomi. Sulla stessa linea di ricerca, il suo gruppo ha giocato anche con la forma delle cellule viventi di Escherichia coli, rendendole più larghe o squadrate, oppure facendole sviluppare in camere di silicone nanofabbricate. In questo modo, i membri del gruppo possono vedere come la forma della cellula influisce sul meccanismo di divisione, e valutare come le proteine Min lavorano in cellule di dimensioni e forma diverse.
“Giochiamo con le tecniche di nanofabbricazione e facciamo cose che un normale biologo cellulare non farebbe mai”, dice. “Ma uno strano biofisico come me può farlo”.
Aggiungere energia al sistema
Ora che è possibile aggiungere componenti alle bolle dei liposomi senza farle scoppiare, i gruppi possono pianificare come far interagire le molecole tra di loro. Quasi tutto ciò che è simile alla vita richiede energia cellulare, di solito sotto forma di ATP. E anche se questa può essere aggiunta dall’esterno per nutrire un sistema sintetico, molti biologi che lavorano su approcci bottom up sostengono che una vera cellula sintetica dovrebbe avere una propria centrale energetica, qualcosa di simile al mitocondrio di una cellula animale o al cloroplasto di una pianta, che producono entrambi ATP.
Il gruppo di Joachim Spatz al Max-Planck-Institut per la ricerca medica di Heidelberg, in Germania, ha costruito un mitocondrio rudimentale in grado di creare ATP all’interno di una vescicola.
Per fare ciò, il suo gruppo ha approfittato delle nuove tecniche microfluidiche. Come prima passo, ha stabilizzato le GUV inserendole all’interno di gocce del tipo acqua-in-olio circondate da un guscio viscoso di polimeri. Poi, mentre queste GUV stabilizzate dalle gocce fluivano lungo un microcanale, il gruppo ha iniettato in esse grandi proteine, all’interno della vescicola o incorporate nella superficie della membrana.
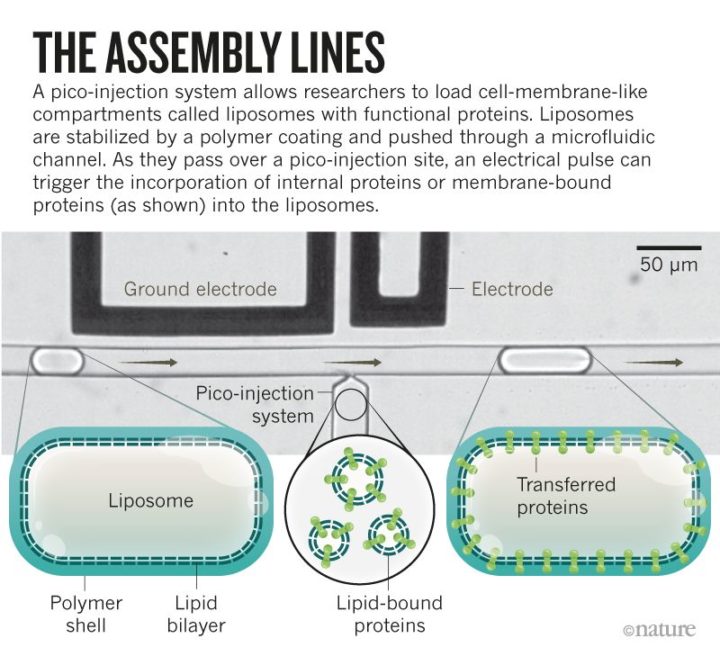
Hanno caricato queste membrane con un enzima chiamato ATP sintasi, che agisce come una sorta di ruota idraulica molecolare, creando energia ATP da precursori di natura molecolare mentre i protoni fluiscono attraverso la membrana. Aggiungendo acido per spingere i protoni fuori dalle GUV, il gruppo ha indotto la produzione di ATP al loro interno.
Spatz spiega che i ricercatori potrebbero far circolare le GUV nel microcanale per un’altra iniezione di proteine, in modo da aggiungere componenti in modo sequenziale. Per esempio, il prossimo passo potrebbe essere aggiungere un componente che imposterà automaticamente il gradiente protonico per il sistema.
“È un modulo importante, come nella vita reale”, afferma Spatz.
Un altro gruppo di biologia sintetica del Max-Planck, guidato dal biochimico Tobias Erb, ha affinato altri approcci per la costruzione di vie metaboliche cellulari. È particolarmente interessato ai percorsi che permettono ai microbi fotosintetici di estrarre anidride carbonica dall’ambiente e produrre zuccheri e altri mattoncini cellulari.
Erb, che dirige un gruppo del Max-Planck-Institut per la microbiologia terrestre a Marburg, in Germania, ha adottato un approccio tabula rasa per sintetizzare vie metaboliche cellulari. “Da un punto di vista ingegneristico, pensiamo a come progettare – dice – e poi costruiamo in laboratorio”.
Il suo gruppo ha delineato un progetto di sistema che potrebbe convertire l’anidride carbonica in malato, un metabolita chiave prodotto durante la fotosintesi. Gli scienziati hanno previsto che questa via sarebbe ancora più efficiente della fotosintesi. Successivamente, Erb e il suo gruppo hanno setacciato alcune banche dati alla ricerca di enzimi che potrebbero eseguire ciascuna delle reazioni. Per alcuni di essi, avevano bisogno di modificare gli enzimi esistenti in quelli progettati.
Alla fine, hanno trovato 17 enzimi di nove diversi organismi, tra cui E. coli, un archaea, la pianta Arabidopsis e gli esseri umani. La reazione, forse non sorprendentemente, era inefficiente e lenta.
“Abbiamo messo in piedi una squadra di enzimi che non hanno giocato bene insieme”, dice Erb. Tuttavia, dopo ulteriore ingegneria enzimatica, il gruppo ha ottenuto una “versione 5.4” che, secondo Erb, ha un’efficienza del 20 per cento superiore a quella della fotosintesi.
Estendendo questo lavoro, il gruppo di Erb ha iniziato a costruire una versione grezza di un cloroplasto sintetico. Tritando spinaci in un frullatore e aggiungendo i suoi macchinari per la fotosintesi al loro sistema enzimatico in provetta, i biologi possono indurre la produzione di ATP e la conversione di anidride carbonica in malato solo illuminandolo con luce ultravioletta.
Tutto potrebbe funzionare in provetta per un breve periodo, dice Erb, “ma alla fine, vorremmo che fosse diviso in compartimenti, come in un cloroplasto”. È entusiasta di collaborare con biologi sintetici come Kate Adamala, che possono costruire e controllare complessi compartimenti.
Il gruppo di Adamala all’Università del Minnesota a Minneapolis, negli Stati Uniti, sta lavorando alla costruzione di bioreattori programmabili, introducendo semplici circuiti genetici nei liposomi e unendoli insieme per creare bioreattori più complessi. Li chiama “bolle di sapone che producono proteine”.
Il suo gruppo costruisce questi bioreattori usando un sistema di tubi stessi simile a quello di Schwille, ma che produce liposomi più piccoli. I ricercatori aggiungono frammenti di DNA circolari chiamati plasmidi che hanno progettato per svolgere una funzione particolare, insieme a tutti i macchinari necessari per produrre proteine dal DNA.
Per esempio, il suo gruppo ha realizzato bioreattori liposomiali in grado di rilevare un antibiotico nel loro ambiente attraverso i pori di membrana e di generare un segnale bioluminescente in risposta.
Unendo sequenzialmente semplici bioreattori, il gruppo può costruire circuiti genetici più complessi. Ma i sistemi iniziano a rompersi mentre si espandono per includere una decina di componenti. Questa è una grande sfida per il settore, afferma Adamala. In una cellula reale, le proteine che potrebbero interferire ciascuna con le azioni dell’altra sono tenute separate da una varietà di meccanismi. Per cellule sintetiche molto più semplici, i biologi devono trovare altri modi per imporre quel controllo. Questo potrebbe avvenire attraverso un gatekeeping esterno, un sistema in cui lo sperimentatore decide quali liposomi si mescolano e quando. Potrebbe anche essere realizzato attraverso etichette chimiche che regolano quali liposomi si possono fondere insieme, o attraverso un sistema di rilascio temporizzato.
Iniezioni d’informazione
Un’altra chiave per creare una cellula è avere il software giusto. Abilitare una cellula sintetica a seguire le istruzioni degli scienziati e replicare se stessa richiederà un modo per archiviare e recuperare informazioni. Per i sistemi viventi, questo viene fatto dai geni: da centinaia per alcuni microbi a decine di migliaia per gli esseri umani.
Di quanti geni una cellula sintetica avrà bisogno per funzionare autonomamente è oggetto di sano dibattito. Schwille e altri vorrebbero limitare il numero a poche decine. Altri, come Adamala, pensano che le cellule sintetiche necessitino di 200-300 geni.
Alcuni hanno scelto di iniziare con qualcosa di vivo. Il biologo sintetico John Glass e i suoi colleghi del J. Craig Venter Institute (JCVI) di La Jolla, in California, hanno preso uno dei genomi microbici più piccoli del pianeta, quello del batterio Mycoplasma mycoides, e hanno sistematicamente interrotto l’attività dei suoi geni per identificare quelli essenziali. Una volta ricevute queste informazioni, hanno assemblato chimicamente un genoma minimo in laboratorio.
Questo genoma sintetizzato conteneva 473 geni – circa la metà rispetto all’organismo originale – ed è stato trapiantato in una specie batterica imparentata, Mycoplasma capricolum. Nel 2016, il gruppo ha dimostrato che questo genoma sintetico minimale potrebbe “avviare” un organismo in grado di vivere autonomamente, anche se a crescita lenta. Glass pensa che sarà difficile far diminuire quel numero ancora di più: se si tolgono tutti i geni, si uccidono le cellule o si rallenta la loro crescita quasi a zero, dice.
Lui e i suoi colleghi del JCVI stanno compilando una lista di “compiti cellulari” basati sull’ultima versione della loro creazione, JCVI-syn3.0a, che potrebbe rappresentare un modello della lista minima delle cose da fare in una cellula. Ma per circa 100 di questi geni non si riesce a identificare la funzione che li rende essenziali.
Come passo successivo, sostenuto da un finanziamento della NSF di quasi un milione di dollari, Glass e Adamala tenteranno di installare il genoma JCVI-syn3.0a in un liposoma sintetico contenente il macchinario necessario a convertire il DNA in proteine, per vedere se può sopravvivere. In quel caso, sia il software sia l’hardware della cellula sarebbero sintetici fin dall’inizio.
Se la cellula potesse crescere e dividersi, sarebbe un passo in avanti incredibile. Ma molti sostengono che per rappresentare veramente un sistema vivente, dovrebbe anche evolversi e adattarsi al suo ambiente. Questo è l’obiettivo dai risultati più imprevedibili e anche dalle sfide più grandi, dice Schwille. “Una cosa che semplicemente produce se stessa per tutto il tempo non è vita; ma sarebbe già un grande risultato!”, dice. “Affinché una cellula sia viva, deve sviluppare nuove funzionalità”.
Il gruppo di Glass al JCVI ha effettuato esperimenti di sviluppo adattativo di laboratorio con JCVI-syn3.0a, selezionando organismi che crescono più velocemente in un brodo ricco di sostanze nutritive. Finora, dopo circa 400 divisioni, Glass e il suo gruppo hanno ottenuto cellule che crescono più velocemente di circa il 15 per cento rispetto all’organismo originale. E hanno visto manifestarsi una manciata di cambiamenti nella sequenza dei geni. Ma non ci sono ancora prove del fatto che il microbo sviluppi nuove funzioni cellulari o aumenti il suo adattamento a passi da gigante.
Erb dice che capire come aggiungere l’evoluzione alle celle sintetiche è l’unico modo per renderle interessanti. Quel po’ di confusione nei sistemi biologici è proprio quello che permette a quei sistemi di migliorare le prestazioni. “Come ingegneri, non possiamo costruire una cellula sintetica perfetta. Dobbiamo costruire un sistema di autocorrezione che migliora via via che funziona”, dice.
Le cellule sintetiche potrebbero portare a intuizioni su come la vita potrebbe apparire su altri pianeti. E i bioreattori sintetici sotto il completo controllo di un ricercatore potrebbero offrire nuove soluzioni per il trattamento del cancro, per combattere la resistenza agli antibiotici o per bonificare i siti tossici. Rilasciare un simile organismo nel corpo umano o nell’ambiente sarebbe rischioso, ma un organismo ingegnerizzato dall’alto verso il basso con comportamenti sconosciuti e imprevedibili potrebbe essere ancora più rischioso.
Dogterom dice che le cellule viventi sintetiche portano anche altre domande filosofiche ed etiche: “Questa sarà vita? Sarà autonoma? La controlleremo? “. Sono conversazioni che dovrebbero avvenire tra scienziati e pubblico, afferma. Riguardo ai dubbi sul funzionamento delle cellule sintetiche, Dogterom è meno preoccupato. “Sono convinto che la nostra prima cellula sintetica sarà una pessima imitazione di quello che già esiste”. E come ingegneri della vita sintetica, con i suoi colleghi possono facilmente incorporare controlli o un kill switch (un interruttore di emergenza) che rende le cellule innocue.
Dogterom e altri biologi sintetici continueranno a spingersi in avanti per esplorare le frontiere della vita. “I tempi sono maturi”, dice. “Abbiamo i genomi, la lista dei componenti. La cellula minima ha bisogno solo di poche centinaia di geni per avere qualcosa che sembri vivo. Centinaia di componenti rappresentano una tremenda sfida, ma non sono migliaia: è molto eccitante.“
(L’originale di questo articolo è stato pubblicato su “Nature” il 7 novembre 2018. Traduzione ed editing a cura di Le Scienze. Riproduzione autorizzata, tutti i diritti riservati.)




Lascia un commento